Из чего состоит атом? Инфографика
 В 1913 году датский физик Нильс Бор предложил свою теорию строения атома. За основу он взял планетарную модель атома, разработанную физиком Резерфордом. В ней атом уподоблялся объектам макромира — планетарной системе, где планеты двигаются по орбитам вокруг большой звезды. Аналогично в планетарной модели атома электроны движутся по орбитам вокруг расположенного в центре тяжёлого ядра.
В 1913 году датский физик Нильс Бор предложил свою теорию строения атома. За основу он взял планетарную модель атома, разработанную физиком Резерфордом. В ней атом уподоблялся объектам макромира — планетарной системе, где планеты двигаются по орбитам вокруг большой звезды. Аналогично в планетарной модели атома электроны движутся по орбитам вокруг расположенного в центре тяжёлого ядра.
Бор ввёл в теорию атома идею квантования. Согласно ей, электроны могут двигаться только по фиксированным орбитам, соответствующим определённым энергетическим уровням. Именно модель Бора стала основой для создания современной квантово-механической модели атома. В этой модели ядро атома, состоящее из положительно заряженных протонов и не имеющих заряда нейтронов, тоже окружено отрицательно заряженными электронами. Однако согласно квантовой механике, для электрона нельзя определить какую-то точную траекторию или орбиту движения — есть только область, в которой находятся электроны с близким энергетическим уровнем.
Что находится внутри атома?
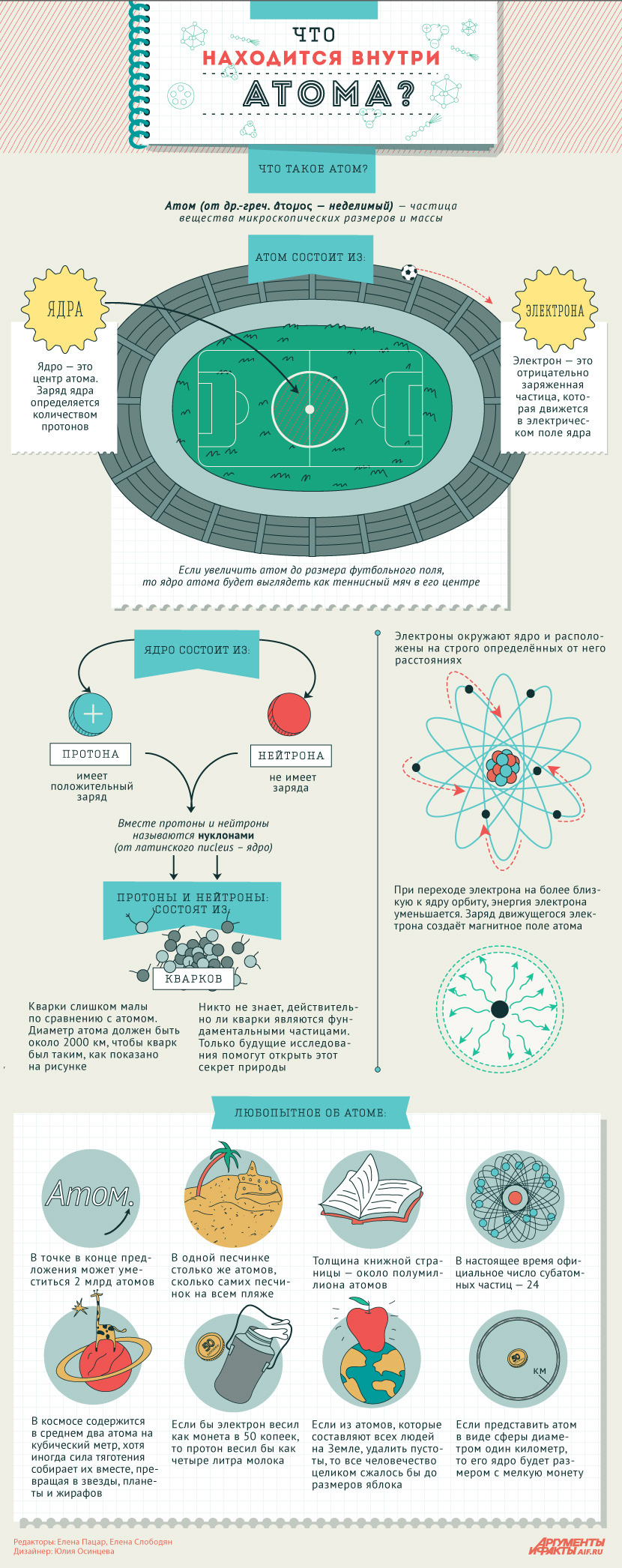
Атомы состоят из электронов, протонов и нейтронов. Нейтроны были открыты после того, как физиками была разработана планетарная модель атома. Лишь в 1932 году, проводя серию опытов, Джеймс Чедвик обнаружил частицы, не имеющие никакого заряда. Отсутствие заряда подтверждалось тем, что эти частицы никак не реагировали на электромагнитное поле.
Само ядро атома образуют тяжёлые частицы — протоны и нейтроны: каждая из этих частиц почти в две тысячи раз тяжелее электрона. Протоны и нейтроны также имеют схожие размеры, но протоны обладают положительным зарядом, а нейтроны не имеют заряда вообще.
В свою очередь, протоны и нейтроны состоят из элементарных частиц, называемых кварками. В современной физике кварки являются самой маленькой, основной частицей материи.
Размеры самого атома во много раз превышают размеры ядра. Если увеличить атом до размеров футбольного поля, то размеры его ядра могут быть сопоставимы с теннисным мячиком в центре такого поля.
В природе существует множество атомов, различающихся размерами, массой и другими характеристиками. Совокупность атомов одного вида называется химическим элементом. На сегодняшний день известно более ста химических элементов. Их атомы различаются размерами, массой, а также строением.
Электроны внутри атома
Отрицательно заряженные электроны двигаются вокруг ядра атома, образуя своего рода облако. Массивное ядро притягивает электроны, но энергия самих электронов позволяет им «убегать» дальше от ядра. Таким образом, чем больше энергия электрона, тем дальше от ядра он находится.
Значение энергии электронов не может быть произвольным, оно соответствует чётко определенному набору энергетических уровней в атоме. То есть энергия электрона изменяется скачкообразно от одного уровня к другому. Соответственно, и двигаться электрон может только в рамках ограниченной электронной оболочки, соответствующей тому или иному энергетическому уровню — в этом смысл постулатов Бора.

Получив больше энергии, электрон «перескакивает» в более высокий от ядра слой, потеряв энергию — наоборот, в более низкий слой. Таким образом, облако электронов вокруг ядра упорядочено в виде нескольких «нарезанных» слоев.
История представлений об атоме
Само слово «атом» происходит от греческого «неделимый» и восходит к идеям древнегреческих философов о наименьшей неделимой части материи. В средние века химики убедились в том, что некоторые вещества не могут быть подвергнуты дальнейшему расщеплению на составляющие элементы. Такие наименьшие частицы вещества и получили название атомов. В 1860 году на международном съезде химиков в Германии это определение было официально закреплено в мировой науке.
В конце XIX — начале XX века физиками были открыты субатомные частицы и стало ясно, что атом в действительности не является неделимым. Сразу же были выдвинуты теории о внутреннем строении атома, одной из первых среди которых стала модель Томсона или модель «пудинга с изюмом». Согласно этой модели, маленькие электроны находились внутри массивного положительно заряженного тела — как изюм внутри пудинга. Однако, практические эксперименты химика Резерфорда опровергли эту модель и привели того к созданию планетарной модели атома.
Развитие планетарной модели Бором наряду с открытием в 1932 году нейтронов сформировало основу для современной теории о строении атома. Следующие этапы в развитии знаний об атоме уже связаны с физикой элементарных частиц: кварков, лептонов, нейтринов, фотонов, бозонов и других.









 Кибервойны: ХХI век принес такие виды оружия, которые могут быть пострашнее атомной бомбы
Кибервойны: ХХI век принес такие виды оружия, которые могут быть пострашнее атомной бомбы  Легенды и мифы вокруг советской атомной бомбы
Легенды и мифы вокруг советской атомной бомбы  Гитлер бы победил, если бы учёные III рейха успели доделать атомную бомбу
Гитлер бы победил, если бы учёные III рейха успели доделать атомную бомбу 

