4 февраля — Всемирный день борьбы против рака. Онкологические заболевания являются одной из причин преждевременной смертности на планете — в возрасте моложе 70 лет — и настоящей проблемой для России и всего мира.
Злокачественные образования органов головы и шеи — довольно редкая онкологическая нозология в структуре общей заболеваемости. Но в структуре смертности она стоит в списке лидирующих позиций, составляя 11-12 тыс. погибших пациентов в год. В России ежегодно регистрируется 35-40 тыс. случаев опухолей органов головы и шеи (исключая рак щитовидной железы), в основном эпителиальных злокачественных новообразований. Опухоли сложно лечатся, обладают высокой агрессивностью, по средней медиане возраста поражают социально активный пласт населения в возрасте 50-60 лет. Чаще заболевают мужчины, но очевиден неуклонный рост заболеваемости среди женщин, поэтому данная онкопатология занимает особое положение в структуре скрининга, ранней диагностики и лечения, рассказала д. м. н., доцент кафедры стоматологии хирургической и ЧЛХ ФГБОУ ВО ПСПбГМУЦ им. академика И. П. Павлова Минздрава России, врач-онколог СПб ГБУЗ «ГКОД» отделения противоопухолевой (лекарственной) терапии № 10 Светлана Кутукова.
Плоскоклеточный рак органов головы и шеи
Эпителиальные злокачественные новообразования органов головы и шеи локализуются в сложной анатомической зоне с различными областями поражения: губа, полость рта, гортань, носоглотка; опухоли ротоглотки со специфическим течением и развитием; опухоли гортаноглотки. В 90% случаев встречается эпителиальное злокачественное новообразование — плоскоклеточный рак органов головы и шеи (ПРГШ), обладающий крайне высокой агрессивностью.
На момент первичной диагностики ПРГШ часто регистрируется в III, иногда в IV стадии заболевания. Выявление ранних признаков болезни и факторов развития ПРГШ — актуальная задача для онкологов и специалистов неонкологического профиля, к которым пациент приходит на первичный прием с любыми жалобами.
От стадии заболевания, на которой диагностирована опухоль, и от ее локализации зависит и показатель смертности. Наименьшая летальность фиксируется при локализации первичной опухоли в области красной каймы губ, как наиболее доступной для визуального контроля и врачу, и пациенту. Но, в целом, ПРГШ имеет высокие показатели летальности на 1-м году от постановки диагноза, и на сегодня снизить эти показатели не удается.
Лишь половина пациентов обращается к врачу в I-II стадии заболевания, когда имеются варианты комбинированного органосохранного лечения; 15% обращаются уже с неоперабельной стадией заболевания. Поэтому, чем раньше врач распознает злокачественный процесс, тем больше шансов у пациента.
Исследования демонстрируют невысокую информированность пациентов о риске заболеваемости злокачественными новообразованиями органов головы и шеи в мире.
Отмечается и низкая настороженность медицинских специалистов. На первичном этапе визуализировать ПРГШ может врач-стоматолог или лор-специалист, к которым пациенты обращаются при появлении каких-либо жалоб. Поздняя диагностика злокачественных новообразований органов головы и шеи происходит и вследствие низкой культуры стоматологического здоровья, низкой информированности пациентов и разнообразия клинических проявлений, что также затрудняет диагностику. Кроме того, возможности ранней диагностики опухолей специалистами нестоматологического или лор-профиля сильно затруднены, поскольку любой другой врач не может заподозрить патологию органов головы и шеи без использования современных методов онкодиагностики.
Эффективная диагностика
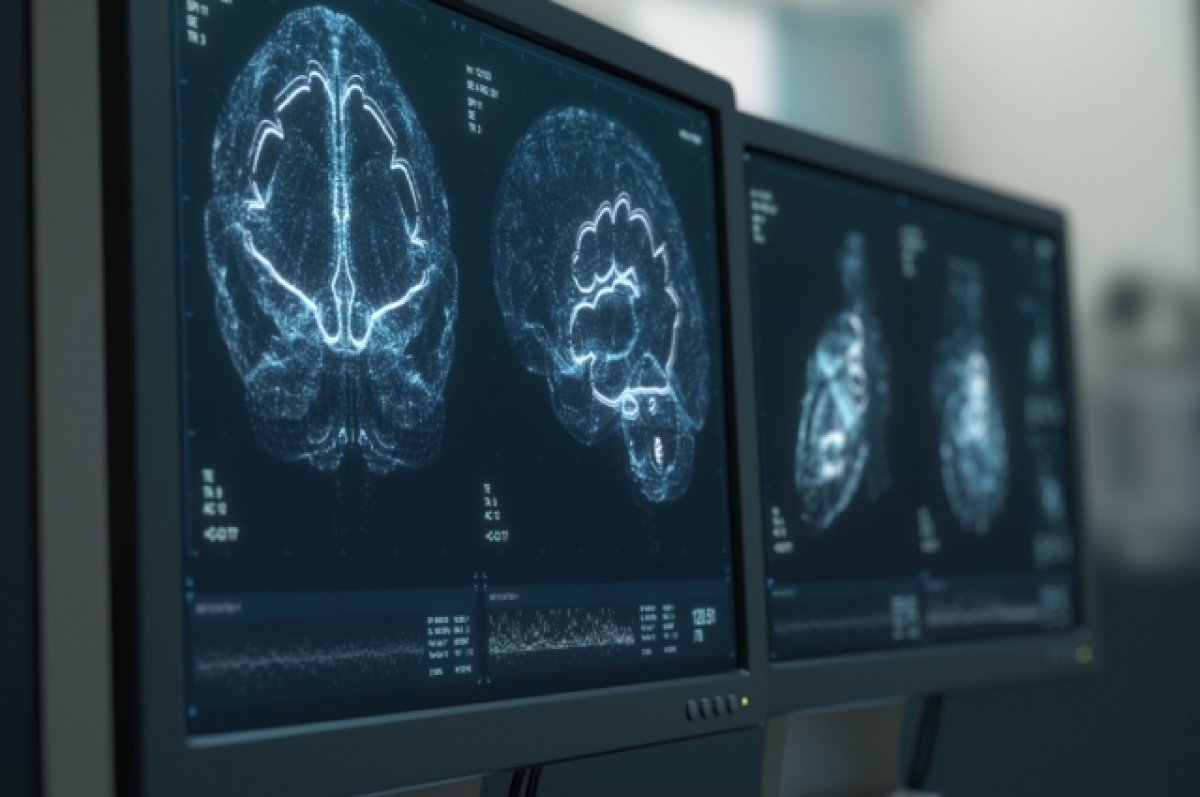
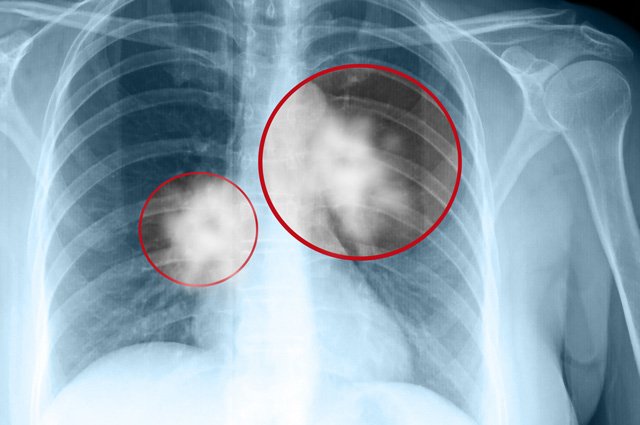
Рентгенологическая диагностика позволяет оценить не только локальные процессы в области конкретного органа или хирургического вмешательства. Обычное стоматологическое или лор-рентгенологическое исследование позволяет оценить состояние большого количества, в т. ч. костных, структур. Спиральная компьютерная или конусная лучевая томография позволяют оценивать достаточное количество структур и заподозрить патологию, в т. ч. в случае заболеваний слизистой оболочки верхнечелюстной пазухи.
Другой простейший метод, доступный для врача любой специализации — пальпация лимфатических узлов у пациента. Неизмененные лимфатические узлы лоцируются в верхней трети шеи, их размер не превышает 1 см, они безболезненны при пальпации, имеют плотную эластическую консистенцию и не собираются в конгломераты. Измененные лимфатические узлы, пораженные метастазами злокачественных новообразований, имеют любую локацию, могут образовывать большие конгломераты.
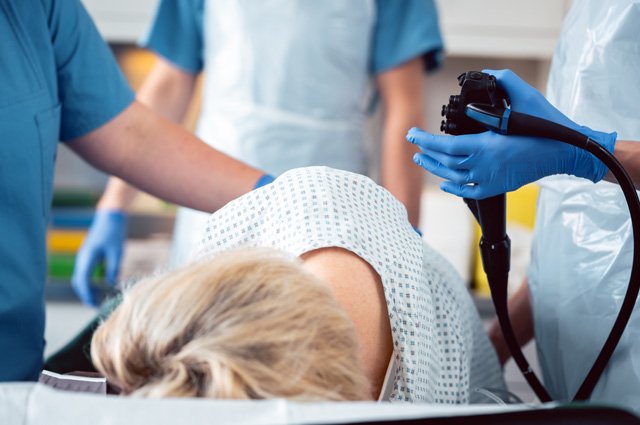
В настоящее время появились инструменты для визуальной оценки в т. ч. слизистой оболочки полости рта и лор-органов. Метод флюоресцентной (люминесцентной) стоматоскопии — диагностики и скрининга ранних форм предопухолевых и опухолевых заболеваний слизистой оболочки полости рта — в 2017 г. законодательно введен в систему обязательного медицинского страхования. Аппарат флюоресцентной стоматоскопии (АФС) должен присутствовать в каждом стоматологическом кабинете и поликлинике, т. к. позволяет на ранних этапах заподозрить дисплазию любой степени, вплоть до злокачественных новообразований. Стоматоскоп АФС позволяет обнаружить патологию за счет света, отражаемого нормальными или измененными тканями. Здоровая слизистая оболочка имеет зеленое или голубоватое свечение, патологически измененная ткань имеет темно-коричневую окраску или не имеет свечения. Метод аутофлюоресцентной эндоскопии может применяться для ранней диагностики и скрининга заболеваний лор-органов, недоступных для простого визуального осмотра. Если имеется возможность направить пациента на подобные исследования, врач должен это сделать.
При первичном использовании метода для обследования 25,5 тыс. пациентов Тульской области у 200 из них были выявлены подозрения на злокачественное образование, у 28 — рак слизистой оболочки полости рта и ротоглотки на ранних этапах, что является необходимым условием для снижения смертности, в т. ч. от этой агрессивной патологии. В г. Санкт-Петербург существует центр ранней диагностики, куда может быть направлен любой пациент на аутофлюоресцентные исследования областей слизистой оболочки полости рта и ротоглотки. Всего за год проведен осмотр более 500 человек, из них 11% направлены с подозрением на развитие злокачественных новообразований.
Основные факторы риска. HPV-ассоциированные опухоли
Один из основных факторов риска в развитии злокачественных новообразований органов головы и шеи — вирус папилломы человека (ВПЧ / HPV). Не все из множества подтипов ВПЧ являются онкогенами и могут вызвать перерождение эпителия и развитие злокачественного образования, но ВПЧ занимает 2-е место среди факторов развития ПРГШ, 100% опухолей ротоглотки ассоциировано с ВПЧ, как правило, 16-го подтипа.
ВПЧ-ассоциированные опухоли ротоглотки имеют высокий рост заболеваемости и, по прогнозам, продолжат демонстрировать тенденцию к увеличению доли ВПЧ-положительных опухолей в структуре эпителиального ПРГШ. Также существует большая когорта больных с ВПЧ-ассоциированными опухолями других отделов головы и шеи. И, если ВПЧ-ассоциация для орофарингеальной зоны имеет более благоприятный прогноз и возможность деэскалации стадии заболевания и лечебных опций, то ВПЧ-ассоциированные опухоли полости рта, например, имеют неблагоприятный прогноз и более агрессивный характер течения.
Сейчас идут дискуссии о вакцинации как способе профилактики. Ее значение доказано для профилактики рака шейки матки, но пока под вопросом эффективность против вирус-ассоциированных опухолей других локализаций, в т. ч. новообразований орофарингеальной зоны, полости рта и гортаноглотки, наиболее часто ассоциированных с ВПЧ. Однако даже на крупных зарубежных конгрессах все чаще встречаются положительные данные о профилактической роли вакцинации для опухолей органов головы и шеи.
Образ жизни как фактор риска
Опухоли головы и шеи очень часто вызываются курением табака. Большинство пациентов, которые обращаются к врачу с опухолями орофарингеальной локализации — рак полости рта, гортани — курят и продолжают курить на момент первичной диагностики злокачественного новообразования, от 50 до 83% больных раком верхних дыхательных и пищеварительных путей продолжают курить после первичной постановки диагноза.
Между тем курение снижает эффективность противоопухолевого лечения. У курящих пациентов также развивается условная резистентность к некоторым лекарственным препаратам, которые в настоящее время применяются при любой стратегии лечения. У курящих пациентов показатели общей выживаемости были значительно ниже, чем у некурящих.
Возможное управление факторами риска в онкологии
Влияние на факторы риска возможно и необходимо. До 80% пациентов не готовы бросить курить немедленно, и необходимо хотя бы снизить негативное влияние курения табака на течение злокачественной патологии и эффективность лечения. Американская ассоциация клинических онкологов разработала рекомендации по ведению пациентов с любыми онкозаболеваниями, которые продолжают курить.
Если у пациента нет готовности или возможности отказаться от табакокурения, можно рекомендовать ему продукцию пониженного риска, например электронные системы нагревания табака (ЭСНТ), которые за счет нагревания, а не горения табака минимизируют вред продуктов горения — токсичного табачного дыма и канцерогенных смол. Продукция пониженного риска станет залогом неразвития злокачественного новообразования верхних дыхательных и пищеварительных путей либо поможет онкологам провести адекватное лечение. У пациентов, отказавшихся от курения или использующих продукцию пониженного риска, наблюдается улучшение биохимических показателей, в т. ч. отвечающих за воспалительные процессы, тромбообразование, оксигенацию тканей. При этом «золотым стандартом» остается полный отказ от курения.
Любой медицинский специалист должен уделять внимание не только основной жалобе таких пациентов, но даже минимальным симптомам, которые могут указывать на наличие онкозаболевания: округлые образования на шее, особенно возникшие более 2 недель назад; жалобы на внезапную или периодически возникающую осиплость голоса; проблемы в полости рта — периодический болевой синдром или неприятные ощущения; уплотнения в области слизистой оболочки полости рта и ротоглотки. Это прямой повод направить пациента на дообследование, чтобы как можно раньше выявить наличие злокачественного новообразования.
Внимательное отношение любых медицинских специалистов даже к незначительным симптомам в области органов головы и шеи поможет раннему выявлению злокачественных опухолей. Также врач любого профиля должен обязательно проводить профилактическую работу с курящими пациентами о вреде курения как факторе риска развития злокачественных поражений, включая опухоли органов головы и шеи, легкого и любых других злокачественных новообразований.